вНвЉЩњЮяЃКеўВпЯђСйДВМБашгУвЉКЭДДаТвЉЧуаБ
ЦРТл
вЉЦЗЦРЩѓИФИяПьЫйЭЦНј,КЫВщеЙЪОжДааСІ:НёФъЯТАыФъПЊЪМ,ЮЊСЫЙцЗЖСйДВЪдбщжЪСПЁЂДђЛїСйДВЪ§ОндьМйЁЂНтОіCDEзЂВсЩъЧыЛ§бЙ,ЙњЮёдКЁЂCFDAеўВпЦЕГіЁЃБОДЮКЫВщКѓЖдВЛКЯИёЩъЧыЕФДІРэЙЋИц,еЙЯжСЫвЉМрОжЭЦНјзЂВсЩѓЦРНјЖШЁЂМгЧПЙцЗЖЛЏЩѓЦРЕФОіаФМАжДааСІЁЃЕБЧАCDEдкЩѓЩъЧывЉЮяга2,1000Иі,дкБрШЫдБ100ЖрШЫ,УПФъЪмРэ8,000~10,000ИівЉЮяЦРЩѓЁЂЭъГЩЩъЧыКХ4,000~5,000ИіЁЃвЊЪЕЯждк2016ФъЕзЧАЯћЛЏЕєЛ§бЙЕФДцСПЁЂЩъБЈЪ§СПКЭЦРЩѓЪ§СПЦНКтЕФФПБъ,ЮвУЧХаЖЯ,СйДВЪдбщКЫВщЕФЗчБЉЛЙНЋМЬај,дкЮДРДаТвЉЦРЩѓИФИяЕФБГОАЯТжа,жЪСПЙмПиЬхЯЕбЯИёЁЂВйзїКЯЙцЕФCROаавЕСњЭЗЙЋЫОНЋМЬајЪмвцЁЃ
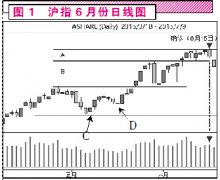
ЙцЗЖСйДВ,бЯГЭдьМй:вЉМрОжзюаТЯТЗЂЕФеўВпдйДЮЧПЕїбЯГЭСйДВЪдбщЪ§ОндьМйЁЃЖдСйДВЪдбщЪ§ОнХЊащзїМйЕФЩъЧыШЫ,здЗЂЯжжЎШеЦ№,3ФъФкВЛЪмРэЦфЩъБЈИУЦЗжжЕФвЉЦЗзЂВсЩъЧы,1ФъФкВЛЪмРэЦфЫљгавЉЦЗзЂВсЩъЧы,вбОЪмРэЕФВЛгшХњзМ,ВЂНјааЮФМўзЗЫнМьВщ,ШчЗЂЯжХЊащзїМйааЮЊ,5ФъФкВЛЪмРэЦфЫљгавЉЦЗзЂВсЩъЧыЁЃЖдВЮгыСйДВЪдбщЪ§ОнХЊащзїМйЕФСйДВЪдбщЛњЙЙ,д№СюЯоЦкећИФ,ећИФЭъГЩЧАВЛНгЪмЦфВЮгыбаОПЕФЩъБЈзЪСЯ,ОећИФШдВЛЗћКЯвЊЧѓЕФ,ШЁЯћЦфЯрЙиЪдбщзЪИёЁЃНќЦкCFDAбЯРїеўВпЦЕЗБГіЬЈ,ЬхЯжСЫеўИЎЖдСйДВЪдбщжЪСПЙмПиЕФОіаФЁЃ
еўВпЯђСйДВМБашгУвЉКЭДДаТвЉЧуаБ:CFDAдк2015Фъ11дТ11ШеЗЂВМЕФЁЖвЉЦЗзЂВсЩѓЦРЩѓХњШєИЩеўВпЁЗжаЬсГі,ЖдаТвЉЕФСйДВЪдбщЩъЧы,ЪЕаавЛДЮадХњзМ,ВЛдйВЩШЁЗжЦкЩъБЈЁЂЗжЦкЩѓЦРЩѓХњЕФЗНЪН,дкЂёЦкЁЂЂђЦкСйДВЪдбщЭъГЩКѓ,ЩъЧыШЫгІМАЪБЬсНЛЪдбщНсЙћМАЯТвЛЦкСйДВЪдбщЗНАИЁЃЮДЗЂЯжАВШЋадЮЪЬтЕФ,ПЩдкгывЉЩѓжааФЙЕЭЈКѓзЊШыЯТвЛЦкСйДВЪдбщЁЃЖдаТвЉСйДВЪдбщЩъЧыЪЕаавЛДЮадЩѓХњ,ЬхЯжГіЖдДДаТвЉЕФжЇГж,гаРћгкЙФРјЦѓвЕНјаабаЗЂДДаТ,РћКУбаЗЂВњЦЗЙмЯпЗсИЛЕФДДаТвЉСњЭЗЦѓвЕЁЃ
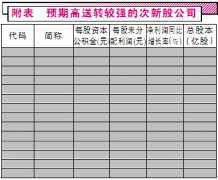
ПЊеЙвЉЦЗЩЯЪааэПЩГжгаШЫжЦЖШЪдЕу,ЪЕаавЉЦЗЩЯЪааэПЩгыЩњВњаэПЩЗжПЊЙмРэ:ЮвЙњФПЧАЪЕаавЉЦЗЩѓХњХњЮФКХжЦЖШ,жЛгавЉЦЗЩњВњЦѓвЕВХПЩвдЩъЧывЉЦЗзЂВс,ШЁЕУвЉЦЗХњзМЮФКХЁЃЮЊЛёЕУХњзМЮФКХ,баЗЂЛњЙЙашвЊПЊЩшЩњВњЯп,ЭЖзЪНЯДѓ;CFDA8дТЗнПЊЪМЬсГівЉЦЗЩЯЪааэПЩГжгаШЫжЦЖШ,11дТПЊЪМЪдЕу,дкетжжЛњжЦЯТ,ЩЯЪааэПЩКЭЩњВњаэПЩЯрЛЅЖРСЂ,дЪаэвЉЦЗбаЗЂЛњЙЙКЭПЦбаШЫдБЩъЧызЂВсаТвЉЁЃЩЯЪааэПЩГжгаШЫПЩвдНЋВњЦЗЮЏЭаЛђепЪкШЈИјЩњВњЩЬЩњВњ,вЉЦЗЕФАВШЋадЁЂгааЇадКЭжЪСППЩПиадОљгЩЩЯЪааэПЩШЫИКд№ЁЃвЉЦЗЩѓХњХњЮФКХжЦЖШЯђЩЯЪааэПЩГжгаШЫжЦЖШЕФзЊБф,НЕЕЭСЫДДаТбаЗЂЕФУХМї,гаРћгкБЃЛЄЗЂУїШЫЕФВњШЈЁЃИУеўВпЛсЬсИпбаЗЂаЭЛњЙЙЛђепИіШЫЕФДДаТЛ§МЋад,РћКУзЈзЂДДаТбаЗЂЕФЧсзЪВњЙЋЫОКЭвНвЉСьгђЕФCMO(КЯЭЌЩњВњзщжЏ)ЙЋЫОЁЃ
ЬсИпЗТжЦвЉЩѓХњБъзМ,ЬсЩ§ВњЦЗжЪСП:2015Фъ11дТ11Ше,CFDAЗЂЮФЬсИпЗТжЦвЉЩѓХњБъзМ,зд2015Фъ12дТ1ШеЦ№,ЗТжЦвЉЩњЮяЕШаЇадЪдбщгЩЩѓХњжЦИФЮЊБИАИжЦ;ЖдЙњФквбгаХњзМЩЯЪаЕФдбавЉ,ЩъЧызЂВсЕФЗТжЦвЉУЛгаДяЕНгыдбавЉжЪСПКЭСЦаЇвЛжТЕФ,ВЛгшХњзМЁЃЗТжЦвЉашвЊНтОіЕФжївЊЮЪЬтЪЧЩѓХњЛ§бЙЁЂЕЭЫЎЦНжиИДМАжЪСПЮЪЬтЁЃвЛжТадЦРМлЪЧНтОіетаЉЮЪЬтЕФживЊЭООЖжЎвЛ,ЭЈЙ§ЗТжЦвЉЕФвЛжТадЦРМл,вЛЪЧЬсИпСЫЦѓвЕГЩБО,ЬдЬСЫВПЗжЫцвтЩъБЈЕФХњЮФ,ЛКНтСЫЛ§бЙ;ЖўЪЧЬсИпСЫВњЦЗжЪСП,дкДЋЭГЕФЙЄвеЛђепЩњВњвЊЧѓЕФЛљДЁЩЯ,діМгСЫЖдВњЦЗаЇЙћЕФвЊЧѓЁЃзюаТЕФеўВпжИв§НЋЩњЮяЕШаЇадЪдбщИќМгЧПЛЏ,ЖдВњЦЗжЪСПЁЂЪдбщбЯНїадЕШЬсГіСЫИќИпЕФвЊЧѓЁЃ
ЭЖзЪНЈвщ
ПДКУДДаТвЉВњвЕСДЁЃздНёФъ7дТЗнПЊЪМ,аТвЉЩѓЦРЗНУцЕФИїжжеўВпЬхЯжСЫеўИЎНтОівЉЦЗзЂВсЛ§бЙЕФОіаФКЭСІЖШ,ЮвУЧдЄМЦНЋЭЦЖЏЙњФквНвЉВњвЕ“ецДДаТ”ЦѓвЕЕФЭЖзЪМлжЕЁЃ
1ЁЂЪзЯШ,дкСйДВЪдбщКЫВщЕФЗчБЉжа,жЪСПЙмПиЬхЯЕбЯИёЁЂВйзїКЯЙцЕФCROаавЕСњЭЗЙЋЫОНЋЛсЪмвц;
2ЁЂЦфДЮ,дквЉЦЗЩѓЦРЩѓХњИФИяБГОАЯТ,МгПьЩѓХњДДаТвЉЁЂЪдЕуЩЯЪааэПЩГжгаШЫжЦЖШЕШДыЪЉНЋРћКУбаЗЂВњЦЗЙмЯпЗсИЛЕФДДаТвЉЦѓвЕЁЂДДаТбаЗЂЛњЙЙЁЂCMOЙЋЫОЕШЁЃ
дкЬсИпЗТжЦвЉЩѓЦРБъзМЕФБГОАЯТ,дЄМЦЛсЬдЬВПЗжЩшЪЉТфКѓЁЂВњЦЗжЪСПНЯВюЕФЦѓвЕЁЃЖдгкЩњВњЩшБИЯШНјЁЂЩњВњЙЄвеЭъЩЦЁЂВњЦЗжЪСПАбПибЯИёЕФЦѓвЕгаРћ,БШШчФЧаЉвбОНЋжЦМСВњЦЗЯњЪлЕНЙцЗЖЪаГЁЕФЦѓвЕЁЃ
ЮвУЧЮЌГжаавЕ“діГж”ЦРМЖ,ЯрЙиЪмвцДњБэадЙЋЫОАќРЈКуШ№вНвЉЁЂЬЉИёвНвЉЁЂОХжовЉвЕЕШЁЃЃЈЙњН№жЄШЏЃЉ
ЩЯвЛЦЊЃКУКЬППЊВЩЃК10дТЗнШЁЕУОјЖдЪевц
ЯТвЛЦЊЃКЭЈаХаавЕЃКаТаЫВњвЕШдЮЊжиЕуВМОжСьгђ
ИќЖр"вНвЉЩњЮяЃКеўВпЯђСйДВМБашгУвЉКЭДДаТвЉЧуаБ"...ЕФЯрЙиаТЮХ
- жЄШЏаавЕЃКОМЭвЕЮёеМБШЛиЩ§ здгЊЙцФЃЛЗБШ
- НЈВФаавЕЃКЮїАВжмБпЪаГЁЕФЫЎФрЗфгЕЖјРД
- ЗПЕиВњЃКзЁЗПЙЋЛ§Н№аХДћзЪВњжЄШЏЛЏвбБЛЬсЩЯ
- гаЩЋаавЕЃКЬМЫсяЎдйДЮДѓЗљЬсМл
- ЭЈаХаавЕЃКЛљДЁЩшЪЉНЈЩшжБНгРћКУЩшБИЩЬКЭЙт
- ЛЗБЃаавЕЃКеўВпвЕМЈЙВеё ЙизЂГЌЖюЪевц
- дьжНЧсЙЄЃКШЫЮФЙмРэДђдьаЃдАЮФОпСњЭЗ
- ЭЈаХаавЕЃКдЫгЊЩЬЕФЧПОЂЭЖзЪЧ§ЖЏТпМШддкГж
- МвЕчаавЕЃКжЧФмЕчЪгВњвЕСДШдЪЧШЋФъЭЦМіЕФЭЖ
- УКЬПаавЕЃКашЧѓШдОЩЕЭУд ЫФМОЖШФббдРжЙл
- Ьхг§аавЕЃКЭјЧђдЫЖЏЕФЦеМАВНЗЅВЛЖЯМгПь
- ЛљДЁЛЏЙЄЃКШ§МОБЈМДНЋТНајХћТЖ ЙизЂяЎЕчГи
- ЭЈаХаавЕЃКЪжЛњЩЯЭјСїСПСЌај9дТЗБЖдіГЄ
- вНСЦЦїаЕЃКЮвЙњЗХСЦЪаГЁгыЙњМЪДцдкНЯДѓВюОр
- ДЋУНаавЕЃКЙњВњЖЏТўНјШыШЋаТЪБЦкЪкШЈЪаГЁЙц
- аТФмдДЃКЗчЕчаТдізАЛњБЃГже§ГЃ
- ЗЧН№ЪєРрНЈВФЃКЛљНЈЭЖзЪЮШдіГЄв§Чц
- ТУгЮаавЕЃКЩёжнзЈГЕгыeДњМнШЗШЯКЯВЂ
- ЙЄвЕ4.0аавЕЃКжаЕЭЖЫЪаГЁОКељИёОжЮДЖЈ
- ЩЬУГСуЪлЃКжаВњНзМЖсШЦ№ЭЦЖЏЯжДњЗўЮёвЕХюВЊ
УПШеВЦЙЩ

- УПШеВЦЙЩЃКЬьАюЙЩЗнЃЈ002124
ЭЖзЪССЕу 1. ЙЋЫОДгЪТТЬЩЋЁЂЛЗБЃаЭЬижжЫЎВњЫЧСЯЕФбаЗЂЁЂЩњВњгыЯњЪл,ЪЧЙњФкЙцФЃНЯ...[ЯъЯИ]