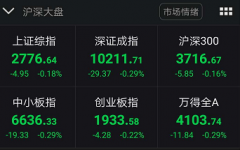
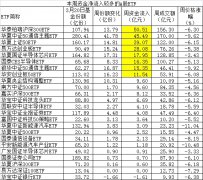
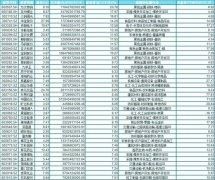
- 2020�й����������½���ԭ��δ����ҵ��չ
- ��Ϊ2019����������٣�ȫ��Ӫҵ����ﵽ85
- �������ε���¼����ٷ���Ӧ3��Ԫ�������
- ��Դ��֭˥��ԭ��Ϊʲôû�б��ɿڿ�����
- ����S20��ʽ���� ����S20��ʽ��������ô��
- �������ں���ʲô���� ��������ô�� �ò���
- ���������˳�MWC��ζ��ʲô?2020�����ƶ�ͨ
- �����Τ������ҵ���������¿�ѧ��˾����ʲ
- ��Ͷ��Ϊʲô��ô������ԭ�������ԭ��
- 2020���й�ҽҩ��ҵ��ǿ��ҵ 2020�й�ҽҩ
ÿ�ղƹ�

- ÿ�ղƹɣ�����ʳƷ(002956)
Ͷ������ 1.��˾����Ӫҵ��Ϊ����ʳƷ���з������������ۡ���˾�Գ�������,ʼ�ռ�...[��ϸ]